近日,湖北大学生命科学学院病毒学与疫苗研究中心陈明周教授团队在合成生物学领域取得重要研究进展,相关成果以 “A synthetic system for RNA-responsive pyroptosis based on type III-E CRISPR nuclease-protease”为题,发表于国际期刊《Nature Communications》。该工作利用合成生物学技术,成功构建了一种基于RNA响应的可编程细胞焦亡诱导系统——DAMAGE系统,为病毒感染、基因突变相关肿瘤及衰老相关疾病等“RNA异质性疾病”的精准干预提供了全新的策略。

图1 论文首页
细胞焦亡是一种由gasdermins(GSDMs)家族蛋白介导的程序性炎症性细胞死亡,在宿主抗感染免疫中扮演重要作用。然而,其天然激活过程受到多重信号通路的严格调控,如何实现可控、靶向的细胞焦亡诱导,是该领域长期面临的技术挑战。
针对上述问题,该团队巧妙地利用III-E型CRISPR系统的核心特征--“RNA识别-蛋白酶激活”级联信号转导,首次将哺乳动物细胞焦亡执行蛋白GSDMs蛋白成功整合进这一原核免疫系统框架中,开发出DAMAGE系统。在该系统中,经截短改造的Csx30蛋白作为“连接子”,将GSDMs的N-端成孔结构域与C-端抑制结构域融合,形成GSDMs-Csx30效应蛋白。当向导RNA(crRNA)引导效应核酸酶Cas7-11识别靶标RNA后,激活Csx29的蛋白酶活性,活化的Csx29随即切割GSDMs-Csx30效应蛋白,释放出具有成孔活性的N端片段,最终精准诱导靶细胞发生焦亡。
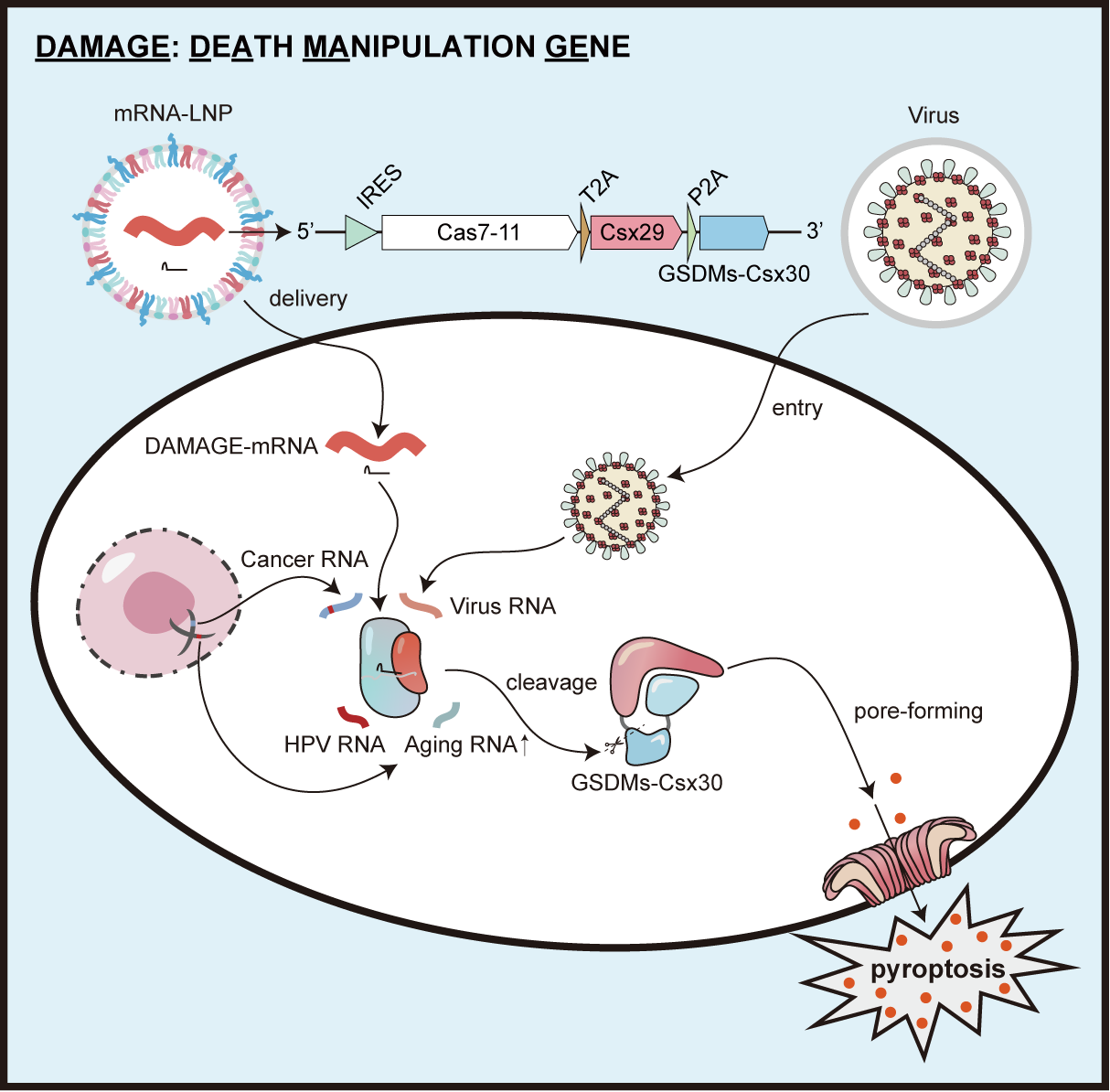
图2 DAMAGE系统:一种RNA靶向性细胞焦亡合成生物学系统
DAMAGE系统展现出三大突出优势:
高特异性:具备单碱基分辨率,可精准区分并清除携带KRAS突变的肿瘤细胞,而对野生型细胞无明显影响;高灵敏度:通过级联信号放大机制,可有效感应细胞内源性低丰度转录本,触发靶细胞焦亡,实现高效杀伤;广适用性和可编程性:通过设计不同的crRNA序列,可灵活靶向多种疾病相关的特异性RNA标志物,展现出应用于RNA异质性疾病的广阔潜力。该研究充分展现了III-E型CRISPR系统在构建可控细胞焦亡通路中的可行性与高效性。目前,该技术已获批国家发明专利。
武汉大学生命科学学院何铭斌博士生和王伟伟博士生为该论文的共同第一作者,湖北大学生命科学学院陈明周教授和覃雅丽教授为共同通讯作者。本研究得到了国家自然科学基金、国家重点研发计划及武汉市自然科学基金等项目的资助(原文链接:https://www.nature.com/articles/s41467-026-69179-5#Abs1)。\
(初审:李爱涛; 终审:黄裕钊)



